Mokslininkai praneša, kad parazitinis kirminas gali slopinti TRPV1+ jutimo neuronus, veiksmingai numalšindamas skausmą ir niežulį odos paviršiuje. Šis atradimas kelia tikslius klausimus apie tai, kaip yra susiję nervų signalai ir imuninės sistemos aptikimas. Jis siūlo biologiniu būdu įkvėptą kelią į neopioidinius analgetikus, taip pat siūlo naujus požiūrius į schistosomiazės prevenciją. Šios pasekmės yra pakankamai reikšmingos, kad būtų galima atidžiai išnagrinėti mechanizmą, saugumą ir perkėlimo potencialą.
Kaip parazitas slopina skausmo signalus

Nors parazitiniai kirminai paprastai siejami su dirginimu, Schistosoma mansoni išsiugdė slaptesnę taktiką: jis išskiria molekules, kurios slopina TRPV1+ baltymus jutimo neuronuose.
Kaip tai leidžia tylų įsibrovimą? Blokuodamas TRPV1+ signalus, parazitas įsiskverbia į odą nesukeldamas skausmo ar niežulio, taip sumažindamas greitą aptikimą ir uždegimą.
Identifikavus slopinančias molekules, būtų galima sukurti neopioidinius analgetikus, kurie taptų gailestingomis priemonėmis slaugytojams. Pelėms atlikti tyrimai rodo, kad TRPV1+ aktyvumas taip pat mobilizuoja apsaugines reakcijas, todėl šios sąveikos supratimas turi dvejopą reikšmę: infekcijos prevencijai ir terapijos mechanizmų panaudojimui.
Vykdomi moksliniai tyrimai siekia nustatyti susijusių molekulių tapatybę ir tikslius neuronų potipius.
TRPV1+ neuronų vaidmuo jutimuose ir imuniteto sistemoje
TRPV1+ jutiminiai neuronai perduoda informaciją apie žalingą karštį, cheminius dirgiklius ir tam tikrus patogenus, o naujausi duomenys rodo, kad jie taip pat formuoja vietines imunines reakcijas.
Kaip šie neuronai perduoda pavojaus signalus ir koordinuoja gynybą? Jie išskiria neuropeptidus, pvz., CGRP ir medžiagą P, kurie moduliuoja kraujagyslių pralaidumą ir mobilizuoja imunines ląsteles. Aktyvacijos modeliai daro įtaką makrofagų ir dendritinių ląstelių elgesiui, nukreipdami citokinų profilius į gijimą arba uždegimą.
Supratimas apie signalų slenksčius gali padėti kurti terapijas, kurios išsaugo organizmo gynybines funkcijas ir tuo pačiu riboja skausmą. Slaugytojams ir gydytojams, pasinaudojant neuronų ir imuninės sistemos sąveika, atsiranda galimybė taikyti intervencijas, kurios palengvina kančias, nepažeidžiant apsauginių funkcijų.
Schistosoma Mansoni: slaptas odos užkariautojas
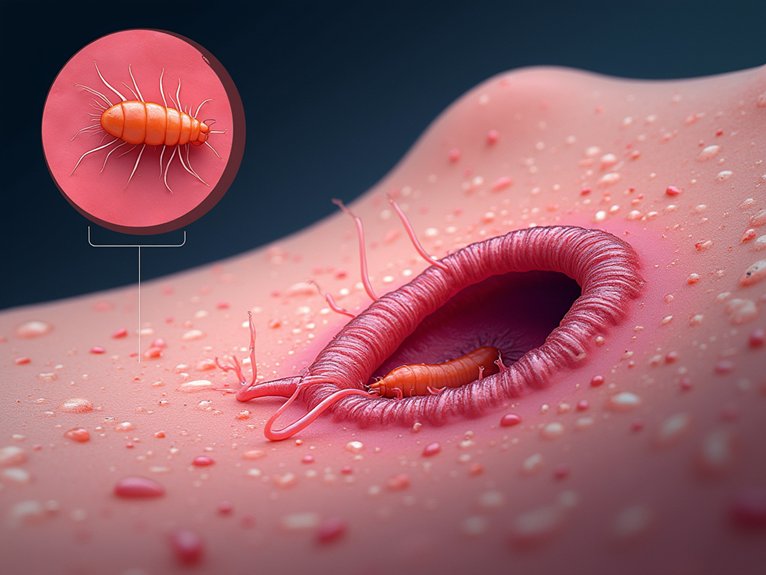
Parazitinis kirminas, Schistosoma mansoni, pasinaudoja subtilia molekuline gudrybe, kad prasiskverbtų pro žmogaus odos apsaugą: jis išskiria veiksnius, kurie slopina jutiminį baltymą TRPV1, silpnindami skausmo ir niežulio signalus, kurie paprastai sukelia greitą imuninės sistemos mobilizaciją.
Stebėtojai klausia, kokios išskiriamos molekulės leidžia tai paslėpti ir kaip TRPV1 blokavimas užkerta kelią ankstyvam uždegimui. Ypač infekcija plinta per kontaktą su užterštu vandeniu atliekant įprastas veiklas, todėl pabrėžiama visuomenės sveikatos svarba ir paslaugomis grindžiama prevencija.
Atradus parazito slopinančius signalus, būtų galima sukurti neopioidinius skausmo gydymo metodus ir parengti tikslingas strategijas, kaip apsaugoti bendruomenes nuo schistosomiazės, stiprinant ankstyvas jutimo ir imunines barjeras.
Eksperimentai, atskleidę nervų slopinimo mechanizmus
Siekiant nustatyti, kaip Schistosoma mansoni slopina odos nocyceptorius, buvo nagrinėjami keli klausimai: kokie molekuliniai signalai išsiskiria susilietus su oda, kokie signalų perdavimo keliai jutimo neuronuose yra tiksliniai ir kaip šie pokyčiai keičia imuninių ląstelių kaupimąsi. Tyrėjai taikė ūmias odos biopsijas, nugaros šaknų ganglių kalcio vaizdinimą ir tikslingus farmakologinius blokatorius, kad nustatytų reakcijas.
Išskirtos proteazės ir lipidiniai mediatoriai buvo izoliuoti ir buvo įrodyta, kad jie mažina neuronų jaudrumą per G-baltymų junginius receptorius ir pasroviui esančias kinazes. Lygiagrečiai atlikti tyrimai kiekybiškai įvertino sumažėjusį chemokinų išsiskyrimą ir pakitusią makrofagų ir neutrofilų chemotaksę. Tyrimų rezultatai parodė, kad prioritetą reikia teikti transliaciniams tyrimams, siekiant panaudoti slopinimo mechanizmus terapiniam skausmo kontrolei.
Kodėl TRPV1+ blokavimas padeda kirminui išgyventi
Daugelis infekcijų pasinaudoja jutimo takais. Kodėl Schistosoma mansoni taiko TRPV1+ neuronus? Slopindamas šį skausmo ir niežulio jutiklį, parazitas riboja neatidėliotinus nervų signalus, kurie paprastai sukelia gd T ląstelių, monocitų ir neutrofilų aktyvaciją.
Sumažėjęs TRPV1+ signalizavimas uždelsta vietinį uždegimą, kuris trukdo lervoms patekti į organizmą, todėl padidėja kirminų galimybė įsiskverbti į odą ir joje apsigyventi. Pelėms atlikti eksperimentai patvirtina evoliucinę atranką šiai slaptumo strategijai.
TRPV1+ slopinimo molekulinės priemonės išaiškinimas galėtų padėti slaugytojams, atskleidžiant intervencijų tikslus, kurie atkuria apsauginį jutimą arba imituoja gerybinį blokavimą terapiniam skausmo kontrolei, suderindami prevenciją su potencialia klinikine nauda.
Sumažėjusio skausmo ir niežulio reakcijų pasekmės imuninei sistemai
Jei TRPV1+ neuronų slopinimas uždelsta minėtus greitus uždegiminius signalus, kokį poveikį tai turi įgimtai ir adaptyviai imuninei mobilizacijai odos barjeroje? Straipsnyje keliamas klausimas, ar sumažėjęs nociceptorių signalizavimas sumažina neutrofilų ir makrofagų mobilizaciją, sutrikdo dendritinių ląstelių aktyvaciją arba pakeičia citokinų aplinką, kuri reguliuoja T ląstelių poliarizaciją.
Jame klausiama, ar sumažėjęs niežėjimas sumažina barjero atkūrimo procesus, pratęsdamas antigeno poveikį ir keisdamas imuninę toleranciją į jautrumą. Apsvarstomos pasekmės vakcinos reakcijoms, antrinėms infekcijoms ir lėtiniam uždegimui. Tonas išlieka tiriamasis, siekiant informuoti slaugytojus ir tyrėjus, ieškančius apsauginių, įrodymais pagrįstų intervencijų.
Parazitų strategijų pavertimas skausmo terapijomis
Schistosoma mansoni išskiriama molekulė, kuri slopina TRPV1+ neuronus, rodo biologiniu būdu įkvėptą kelią į neopioidinius analgetikus. Tyrėjai klausia, kurie helminth faktoriai selektyviai blokuoja TRPV1+ signalizavimą ir ar sintetiniai analogai gali atkurti analgeziją be imuninės sistemos slopinimo.
Ar identifikuotos molekulės gali tapti vietiniais ar sisteminiais preparatais, skirtais skausmui ir niežėjimui malšinti, tuo pačiu išsaugant organizmo gynybines savybes? Tyrimai turi suderinti veiksmingumą su apsauginių imuninių ląstelių, kurias paprastai mobilizuoja TRPV1+ aktyva
Transliacinis darbas reikalaus apibrėžti molekulinės taikinius, dozes, pristatymą ir saugumą. Tokie pastangos galėtų duoti gailestingas terapijas, kurios sumažintų priklausomybę nuo opioidų ir padėtų pacientams, turintiems chroniško skausmo poreikius.
Šistosomiazės prevencijos perspektyvos naudojant neuroninius tikslus
Ar nervų takų, kuriuos sutrikdė Schistosoma mansoni, taikymas galėtų būti naujas būdas užkirsti kelią infekcijai ar sumažinti jos plitimą? Tyrėjai svarsto, ar modifikuojant šeimininko jutimo ar autonomines grandines būtų galima pakeisti parazitų patekimą, migraciją ar kiaušinėlių išsiskyrimą.
Tyrimai gali padėti nustatyti neuroninius signalus, kurie daro įtaką odos barjero apsaugai, imuninės sistemos aktyvinimui arba kraujagyslių pokyčiams, palengvinantiems kirminų įsikūrimą. Tokiais mechanizmais pagrįstos intervencijos galėtų papildyti vakcinas ir sanitarijos priemones, teikiant pirmenybę bendruomenės naudai ir pritaikymui.
Tyrimai būtų sutelkti į išmatuojamus galutinius rezultatus – sumažėjusį infekcijų skaičių, mažesnį kiaušinių kiekį arba sumažėjusį cerkarijų skverbtį – tuo pačiu įtraukiant visuomenės sveikatos suinteresuotas šalis, kad moksliniai tikslai būtų suderinti su paslaugomis orientuotu įgyvendinimu.
Terapijos plėtros iššūkiai ir saugumo aspektai
Prieš pradedant klinikinį parazitų kilmės TRPV1 moduliavimo intervencijų naudojimą, reikia išspręsti keletą svarbių saugos ir perkėlimo į klinikinę praktiką klausimų. Svarbiausias iš jų yra dozės tikslumas: norint imituoti kirmino skausmą slopinančią veiklą, nesukeliant plačios TRPV1 priklausomos nocicepcijos ir termoreguliacijos slopinimo, reikia labai selektyvių agentų ir pristatymo strategijų.
Kaip kūrėjai gali užtikrinti tikslinį TRPV1+ slopinimą, išsaugodami apsaugines jutimo ir imunines funkcijas? Kokie ikiklinikiniai modeliai atskleis netikslius ir lėtinius poveikius? Reguliavimo institucijos reikalaus griežtų saugumo, dozavimo ir veiksmingumo duomenų apie šią naują klasę. Balanso tarp kančių palengvinimo ir sutrikusios organizmo apsaugos prevencijos išlaikymas lieka pagrindiniu etiniu ir moksliniu imperatyvu.
Kiti tyrimų etapai ir galimas klinikinis poveikis
Kiti tyrimų etapai ir galimas klinikinis poveikis
Remdamiesi saugumu ir transliacijos kliūtimis, mokslininkai dabar turi numatyti konkrečius tolesnius žingsnius, kurie lems, ar parazitų kilmės TRPV1 moduliatoriai galės būti naudojami klinikinėje praktikoje. Jie identifikuos ir izoliuos S. mansoni išskiriamas molekules, kurios blokuoja TRPV1, apibūdins jų cheminę sudėtį ir išbandys veiksmingumą neuroninių takų modeliuose.
Lygiagrečiai atliekami darbai padės apibrėžti gd T ląstelių potipius, kurie tarpininkauja atsakams, ir išsiaiškinti, kaip helmintai išvengia aptikimo, atskleidžiant terapinius pažeidžiamumus. Transliaciniai prioritetai apima ikiklinikinį saugumą, aktyvių junginių sintezę ir opioidų nenaudojančių skausmo tyrimų dizainą. Kiekviename etape keliamos pragmatiškos, etikos principais grindžiamos klausimai apie naudą, riziką ir paslaugas pacientams bei bendruomenėms.